

聚克®是由三种人体正常生理菌株组成的活菌制剂,其中包括两株不同的鼠李糖乳杆菌以及一株屎肠球菌。
鼠李糖乳杆菌主要定植在回肠(图1),屎肠球菌主要定植在盲肠及横结肠处(图2)。
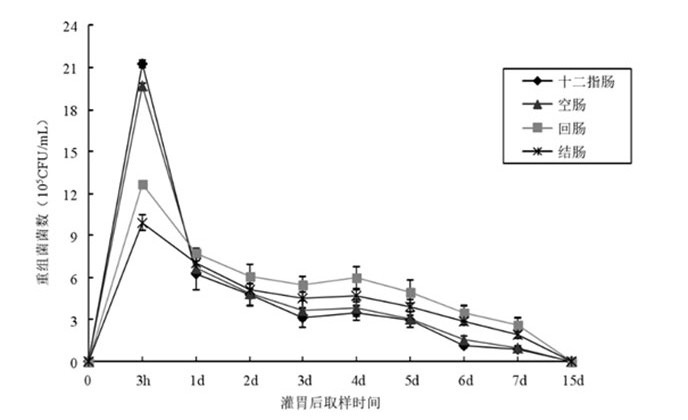
图1 小鼠各肠道内新定植鼠李糖乳杆菌数量
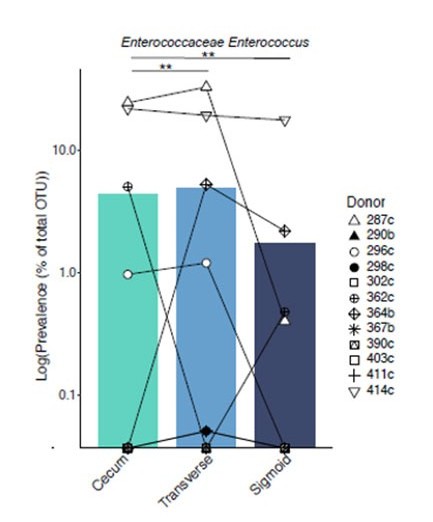
图2 屎肠球菌在大肠中的分布
1 Li C, Bei T, Niu Z, et al. Adhesion and Colonization of the Probiotic Lactobacillus rhamnosus Labeled by Dsred2 in Mouse Gut. Curr Microbiol. 2019;76(7):896-903.
2 James KR, Gomes T, Elmentaite R, et al. Distinct microbial and immune niches of the human colon. Nat Immunol. 2020;21(3):343-353.
抗生素耐药因子:许多活菌(包括有益菌)带有抵抗抗生素的耐药因子,可以在抗生素的环境中生存。但很多情况下这种耐药因子具有外传的风险,使得肠道内有害活菌获得这种耐药因子,而使抗生素治疗疾病的有效性下降,给病人带来风险。
聚克®使用的所有菌株经过中国科学院微生物研究所、上海交通大学生命科学院、中国药科大学等单位的研究,在拟肠道环境实验中没有发现耐药因子转移现象,另外基于现代科技的生物信息学手段,将三代全基因组测序的结果按照欧盟食品安全标准比对抗性基因数据库,没有发现可发生的抗生素耐药因子水平转移的分子生物学基础,复合乳酸菌肠溶胶囊所使用的所有的菌株均符合欧盟食品标准的抗生素耐药因子不转移的安全要求。
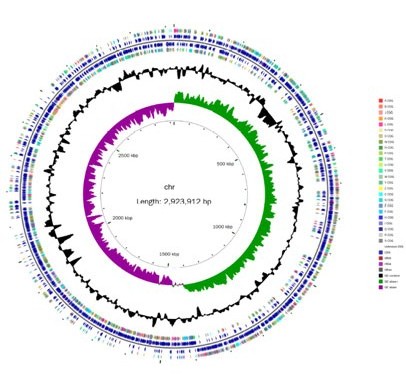
图3 鼠李糖乳杆菌Ⅰ株(Ll)核基因组圈图
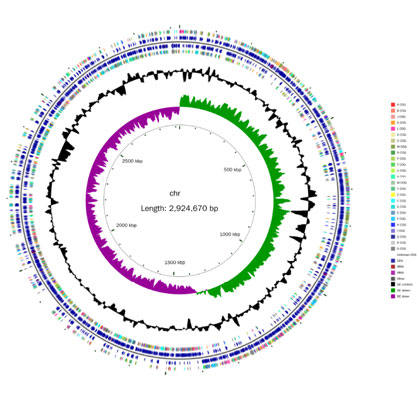
图4 鼠李糖乳杆菌II株(La)核基因组圈图
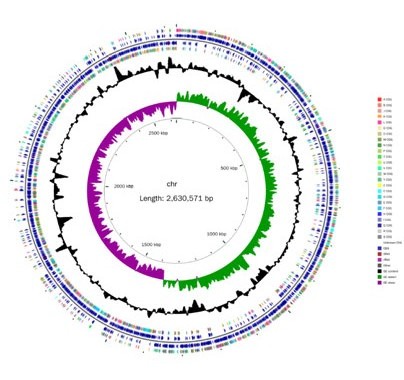
图5 屎肠球菌核基因组圈图
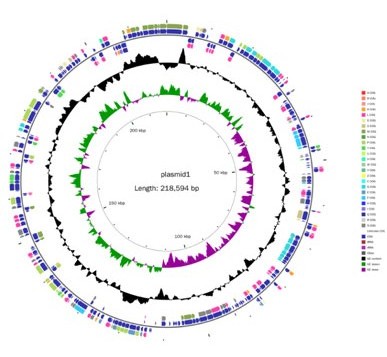
图6 屎肠球菌质粒基因组圈图
鼠李糖乳杆菌可与肠道菌群发生相互作用,提高有益菌占比,维护肠道内环境稳态。比如鼠李糖乳杆菌虽不直接产生短链脂肪酸(short-chain fatty acids, SCFAs),但是可以增加肠道中产短链脂肪酸的菌的数量,间接提高小肠及血清中SCFA的浓度 。
鼠李糖乳杆菌有较强的抵抗致病菌在人体内定植的能力。首先鼠李糖乳杆菌本身便对肠粘膜细胞有很好的粘附性,可优先占据物理位置,其次鼠李糖乳杆菌作为乳酸菌的一种具有很强的产有机酸的能力,可产生对致病菌不利的小环境。再次鼠李糖乳杆菌可与致病菌竞争类似的营养需求,迫使其使用效率更低的代谢 。故而鼠李糖乳杆菌可通过多途径降低致病菌在人体中的竞争力,阻止其定植,加速其排出。
鼠李糖乳杆菌可帮助保护肠道,维持肠道屏障的完整性。加入了鼠李糖乳杆菌的肠道组织片段,即使在炎症因子的影响下也能相对较好地保持住内容物不让其渗出。这种保护作用与紧密连接蛋白occludin、ZO-1有关 。
鼠李糖乳杆菌产生的某些小分子物质可通过脑肠轴影响机体。比如鼠李糖乳杆菌JB-1的长期喂养会诱导小鼠大脑中GABAB1b及GABAAα2mRNA的表达改变,减少压力诱导的皮质酮以及焦虑和抑郁相关的行为 。
鼠李糖乳杆菌有免疫调节功能。比如LGG的外分泌蛋白p40及p75通过激活表皮生长因子受体(EGFR)和下游PI3K/Akt和PKC信号通路,帮助肠上皮细胞抵抗细胞凋亡;LGG的纤毛(pili)可减弱由于与细菌的相互作用而导致的白细胞介素-8 (interleukin-8,IL-8)的产生 。
鼠李糖乳杆菌可产生一些人体不具备的生物酶,帮助人体进行代谢。比如低聚半乳糖可促进鼠李糖乳杆菌的生长,增加宿主体内β-半乳糖苷酶的含量,缓解乳糖不耐症 。
1.BerniCanani R, Sangwan N, Stefka AT, et al. Lactobacillus rhamnosus GG-supplemented formula expands butyrate-producing bacterial strains in food allergic infants. ISME J. 2016;10(3):742-750.
2.Alonso-Roman R, Last A, Mirhakkak MH, et al. Lactobacillus rhamnosuscolonisation antagonizes Candida albicans by forcing metabolic adaptations that compromise pathogenicity. Nat Commun. 2022;13(1):3192. Published 2022 Jun 9.
3.Han X, Lee A, Huang S, Gao J, Spence JR, Owyang C. Lactobacillus rhamnosus GG prevents epithelial barrier dysfunction induced by interferon-gamma and fecal supernatants from irritable bowel syndrome patients in human intestinal enteroids and colonoids. Gut Microbes. 2019;10(1):59-76.
4.Bravo JA, Forsythe P, Chew MV, et al. Ingestion of Lactobacillus strain regulates emotional behavior and central GABA receptor expression in a mouse via the vagus nerve. Proc Natl Acad Sci U S A. 2011;108(38):16050-16055.
5.van Baarlen P, Wells JM, Kleerebezem M. Regulation of intestinal homeostasis and immunity with probiotic lactobacilli. Trends Immunol. 2013;34(5):208-215.
6.Arnold JW, Simpson JB, Roach J, Bruno-Barcena JM, Azcarate-Peril MA. Prebiotics for Lactose Intolerance: Variability in Galacto-Oligosaccharide Utilization by Intestinal Lactobacillus rhamnosus. Nutrients. 2018;10(10):1517. Published 2018 Oct 16.